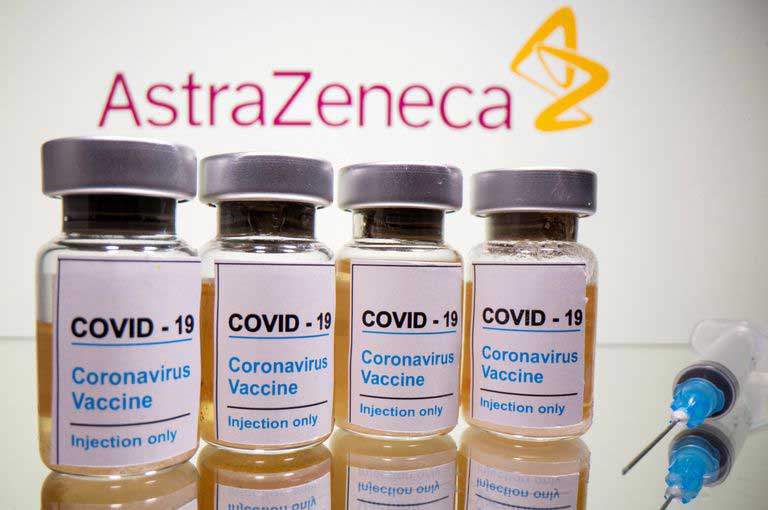
Berlín. La Comisión de Vacunación alemana recomienda, en un informe no definitivo difundido ayer, limitar a menores de 65 años el uso de la vacuna de AstraZeneca contra el coronavirus, que podría ser aprobada hoy por la Agencia de Medicamentos Europea (EMA).
“No hay de momento datos suficientes para juzgar la efectividad de la vacuna en mayores de 65 años”, según la versión del informe de la Comisión de Vacunación del que informaron medios locales. El ministro de Sanidad, Jens Spahn, matizó tras divulgarse esa opinión que la recomendación de la comisión sobre AstraZeneca no es definitiva, sino sólo una propuesta provisional.
Agregó que la decisión final se tomará solamente una vez que la EMA se pronuncie positivamente sobre la vacuna de AstraZeneca y que la Comisión Europea la autorice. La vacuna de AstraZeneca todavía no tiene la aprobación europea, pero se espera que pueda conseguirla mañana.
En el caso de que se confirmara la recomendación del organismo alemán podría emplearse la vacuna de manera prioritaria con personal médico y sanitario o para personas de entre 60 y 65 años, avanzan medios alemanes.
En una evaluación provisional publicada en diciembre en la revista “The Lancet” de un estudio con 11,636 personas se comprobó que la vacuna de AstraZeneca tenía una efectividad de entre el 60 y 90 % aunque el fabricante indica que la efectividad ronda el 70 %.
No obstante, la gran mayoría de personas que participaron en el estudio tenían un máximo de 55 años y solo un pequeño grupo, un 8 %, pertenecía la franja de edad de entre 56 y 69 años.
EMA anuncia hoy sus conclusiones
EMA publicará hoy sus conclusiones de la evaluación de la vacuna del COVID-19 desarrollada por AstraZeneca y la Universidad de Oxford, y subrayó que solo le dará luz verde si los datos presentados por la farmacéutica son “lo suficientemente sólidos y completos”.
La EMA subrayó que si el paquete de datos se lo permite, y la empresa “presenta rápidamente cualquier información adicional necesaria para completar la evaluación” en las próximas 24 horas, el comité de medicamentos humanos (CHMP) “podría emitir” una recomendación a la Comisión Europea sobre una posible autorización de esta vacuna este mismo viernes.
Los detalles de su análisis científico se harán públicos en torno a las 15.00 hora neerlandesa (14.00 GMT), desde su sede en Ámsterdam, con una rueda de prensa virtual en la que su directora, Emer Cooke, y otros jefes de departamentos como el de Vacunas y el de Seguridad, explicarán la evaluación de los datos de laboratorio y los ensayos clínicos hechos con este fármaco.
La EMA lleva semanas analizando los datos sobre el proceso de producción, los ingredientes, la calidad, la seguridad y la eficacia de esta vacuna de COVID-19, que, de lograr el visto bueno de los científicos europeos, sería el tercer antídoto aprobado en la Unión Europea (UE) contra el covid-19, después del de Pfizer/BioNTech y Moderna, que consiguieron su licencia condicional el 21 de diciembre y el 6 de enero respectivamente.
ONU denuncia la falta de solidaridad
El secretario general de la ONU, António Guterres, denunció la falta de solidaridad que se está dando con las vacunas de la covid-19, por el momento disponibles únicamente en algunos países y totalmente inaccesibles en las naciones más pobres. “La ciencia está teniendo éxito, pero la solidaridad está fallando”, subrayó Guterres en un discurso ante la Asamblea General.