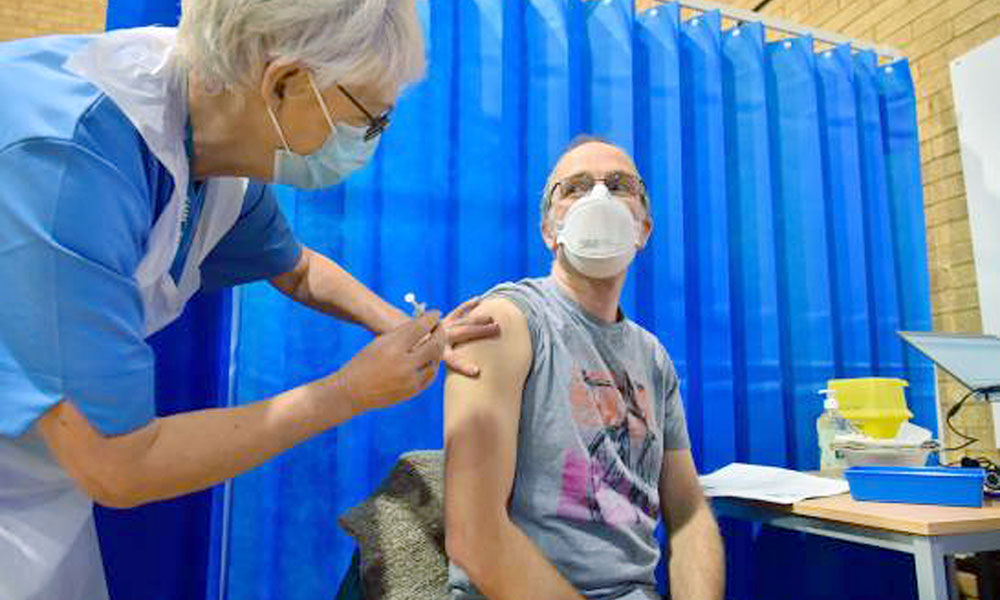
Londres. Los reguladores del Reino Unido han aprobado para su uso en este país la vacuna contra la covid-19 desarrollada por la Universidad de Oxford y la farmacéutica AstraZeneca, informó ayer miércoles el ministerio de Sanidad.
La Agencia Reguladora de Productos Sanitarios y Médicos (MHRA, por sus siglas en inglés) ha dado el visto bueno a este preparado, el segundo que entra en el programa de inmunización contra el coronavirus iniciado el pasado día 8 en el Reino Unido.
Además de la vacuna de Oxford/AstraZeneca, considerada segura y efectiva, el país está vacunando con la de Pfizer/BioNTech.
El Reino Unido ya tiene comprometidas cien millones de dosis del preparado de Oxford/AstraZeneca, que permitirá vacunar a 50 millones de personas, ya que se necesitan dos dosis.
En un comunicado, el ministerio de Sanidad indicó que el Gobierno aceptó la recomendación de los reguladores de utilizar esta vacuna después de “unos ensayos clínicos rigurosos” y “un análisis de los datos por parte de expertos de la MHRA”.
Los reguladores, añadió el ministerio, concluyeron que la vacuna “cumple con estrictos niveles de seguridad, calidad y efectividad.
Los datos publicados a principios de diciembre en la revista médica “The Lancet” indicaron que la vacuna es efectiva en un 62 % cuando se suministra dos dosis completas de la vacuna, pero que la efectividad asciende al 90 % cuando se suministra la mitad de la primera dosis seguida de una completa en la segunda.
EEUU la distribuirá hará en abril
Mientras, que en Washinton, DC, la agencia reguladora de fármacos de EE.UU. dijo que espera autorizar en abril la distribución de la vacuna desarrollada por la farmacéutica británica AstraZeneca y la Universidad de Oxford, indicó ayer miércoles Moncef Slaoui, principal asesor de la Operación Warp Speed.
“Esperamos que si todo va bien con la revisión, la autorización de uso de emergencia se pueda otorgar en algún momento en abril”, manifestó en una rueda de prensa Slaoui, quien se encarga de dirigir la Operación Warp Speed, organizada por la Casa Blanca y el Pentágono para acelerar la campaña de inmunización.
Lo que se le otorgaría a AstraZeneca, explicó Slaoui, sería una “autorización de emergencia”, es decir, un permiso extraordinario que servirá para acelerar la distribución de la vacuna contra la covid-19, mientras se siguen recolectando más datos para dar el visto bueno definitivo.
El asesor Moncef Slaoui explicó que ya se ha reclutado a 29.000 voluntarios en Estados Unidos para probar la eficacia de la vacuna.